动物研究所合作揭示灵长类动物发育和寿命调控的关键通路
来自中国科学院动物研究所、生物物理研究所、干细胞与再生医学创新研究院的研究团队联合攻关,经过三年的不懈努力,首次实现了SIRT6在非人灵长类动物中的全身敲除,获得了世界上首例特定长寿基因敲除的食蟹猴模型。与SIRT6敲除小鼠表现的加速衰老表型明显不同,SIRT6敲除的食蟹猴在出生数小时内即死亡。多项分析结果显示,SIRT6敲除的食蟹猴未见加速衰老表型,却表现出严重的全身发育迟缓。新生SIRT6敲除猴的脑、肌肉及多种其他器官组织均表现出明显的胚胎期未成熟的细胞和分子特征。此外,利用人类干细胞模型开展的研究表明,SIRT6缺乏也可阻滞人类神经干细胞向神经元的分化。进一步的分子机制研究发现,SIRT6可以通过介导长链非编码核糖核酸H19印记调控区的组蛋白去乙酰化来反式抑制H19的表达,而SIRT6的缺乏则会在灵长类动物神经前体细胞中引起H19表达的异常上调,进而导致脑发育迟缓。
该成果在2018年8月22日在线发表于国际顶尖学术期刊Nature。该研究首次结合非人灵长类动物模型、人类干细胞模型及基因编辑技术揭示了可调控灵长类动物出生前发育程序的关键分子开关,为研究人类出生前发育迟缓综合征提供了重要的模型体系。此外,该研究首次揭示了灵长类和啮齿类动物在衰老调节通路方面的巨大差异,为开展人类发育和衰老的机制研究,以及相关疾病的干预奠定了重要的基础。
该研究工作由中国科学院动物研究所、中国科学院生物物理研究所、中国科学院干细胞与再生医学创新研究院、首都医科大学宣武医院、北京大学附属第一医院、和中山大学等机构合作完成。中国科学院动物研究所胡宝洋研究员、李伟研究员和中国科学院生物物理研究所刘光慧研究员为论文的共同通讯作者。中国科学院生物物理研究所张维绮研究员,中国科学院动物研究所万海峰助理研究员、冯桂海副研究员和曲静研究员为共同第一作者。周琪院士对工作的开展给予了重要的支持和指导。该研究受到中科院“器官重建与制造”战略科技先导专项及科技部、基金委等项目的资助。(论文链接)
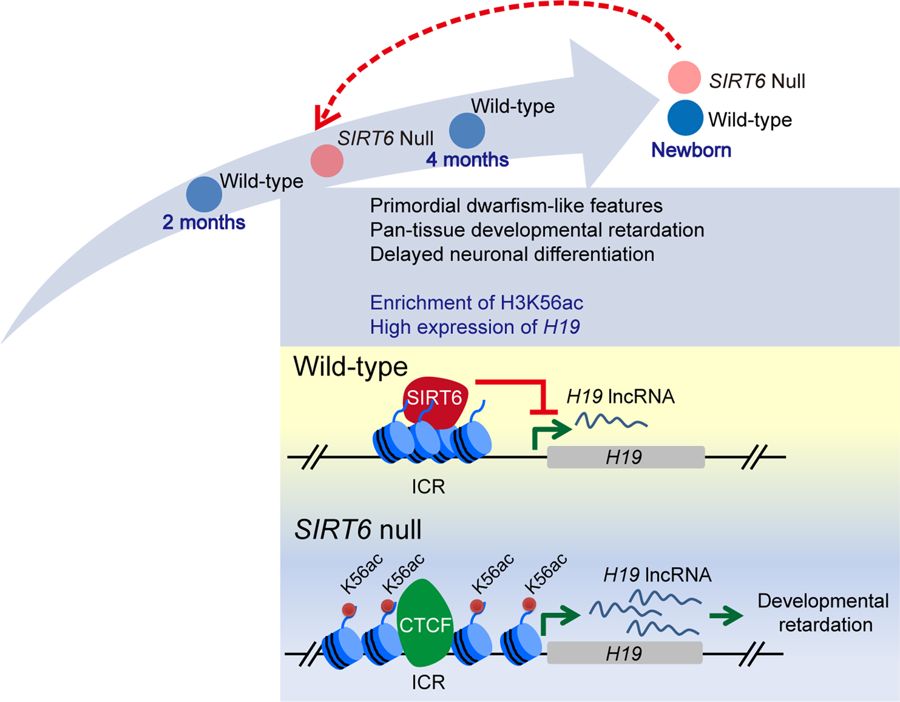
SIRT6调控猴胎儿发育机制模型
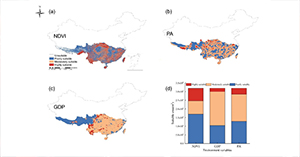
人类活动和气候变化加速生物多样性的减少,导致物种范围的转移、收缩和扩张。在全球范围内,人类活动和气候变化已对生物多样性构成了严重威胁,目前已导致全球522种灵长类动物中约68%的物种面临灭绝风险。

植物病毒素有“植物顽疾”之称,每年引起全球作物经济损失高达4000亿元。水稻作为人类重要的粮食作物之一,供给全世界一半以上的人口,主要种植于亚洲、非洲和南美洲等地区。

