王金勇研究组开发NKP肿瘤治疗新技术
CAR-NK细胞在疾病治疗中展现出安全和通用的优势,但疗效不理想。临床上,为了提高CAR-NK细胞疗效,多采用高剂量、多剂次输注给药的策略,这导致治疗成本显著增加,加重患者经济负担。因此,传统的人体组织来源CAR-NK细胞疗法面临疗效和成本问题双重挑战。
2026年2月24日,中国科学院动物研究所器官再生与智造全国重点实验室王金勇研究组在干细胞领域专业刊物Cell Stem Cell以长文形式在线发表了题为“Pluripotent stem cell-derived CAR-NK progenitor therapy targets minimal residual disease and prevents relapse in leukemia models”的最新研究成果(图1)。研究团队开发出多能干细胞诱导来源的CAR‑iNK祖(CAR-iNKP)细胞疗法,实现体内大规模产生持续时间久的CAR-iNK细胞。传统化疗联合低剂量、单一剂次的CAR-iNKP细胞输注就可在人类B-ALL和T-ALL肿瘤动物模型上实现有效清除肿瘤微小残留病灶,显著降低肿瘤复发率。该项研究成果为传统CAR-NK细胞疗法面临的体内存续时间短、长期疗效不足等问题提供了新技术解决路径。
长期以来,王金勇研究组致力于开发“体外育种,体内发育成熟”的两步法再生血液/免疫细胞策略,并建立气液交界面的“类器官培养法”大规模制备iNK细胞的技术工艺。该研究通过对类器官培养系统诱导iNK细胞再生体系开展单细胞级别的时空动态分析,成功鉴定出与天然NKP细胞(Virginie M. Renoux, et al. 2015 Immunity)表型和功能相似的细胞群体,并将其定义为iNKP细胞。
随后,研究人员构建了表达CXCR4(CXCL12受体)的hPSC(R4-PSC)细胞系,并体外诱导其分化获得具有骨髓归巢能力的NK细胞种子—R4-iNKP细胞。通过尾静脉输注低剂量R4-iNKP细胞到IL15人源化小鼠(B-NDG hIL15小鼠,20万R4-iNKP/只),细胞归巢至骨髓,经7-10天在骨髓微环境中发育成熟为R4-iNK细胞,并进入血液循环系统和肝脏、淋巴结、脾脏、肺脏等多个实体脏器。令人鼓舞的是,这种体内再生策略实现iNK细胞在外周血液循环系统持续存在80天以上。表达CAR的R4-iNKP细胞同样能体内产生CAR-R4iNK细胞,并且在外周血液循环系统中存在超过80天(图2)。
为了评估CAR-R4iNKP细胞治疗肿瘤的转化潜力,研究人员选择了CAR-T细胞治疗领域的经典靶点CD19和CD7,分别测试CAR-R4iNKP细胞疗法抗B急淋(B-ALL)和T急淋(T-ALL)肿瘤的效果。研究人员首先测试CAR-R4iNKP细胞体内产生的CAR-R4iNK细胞能否预防肿瘤发生。在B-NDG hIL15小鼠中输注20万个CAR‑R4iNKP细胞,待2~3周后再注射CD19阳性的NALM6肿瘤细胞或CD7阳性的CCRF‑CEM肿瘤细胞来模拟肿瘤发生场景。结果表明,所有实验组小鼠均成功抵御肿瘤接种挑战,而未输注CAR‑R4iNKP的对照组小鼠全部发生肿瘤。因此,体内分化产生的CAR‑R4iNK细胞能够有效抵抗肿瘤接种的挑战,具备一定的精准免疫监视肿瘤发生的功能。
化疗后复发是临床治疗恶性肿瘤的痛点。为评估CAR‑R4iNKP细胞清除化疗后肿瘤微小残留病灶(MRD)的潜力,该研究进行了化疗联合CAR-R4iNKP细胞输注方案清除MRD的概念验证。结果显示化疗联合低剂量、单一剂次的CD19CAR‑R4iNKP细胞输注,可以在人类B-ALL肿瘤动物模型上实现长期零复发。同样方案也可实现T-ALL肿瘤复发率降低50%,剩余复发小鼠的生存期也显著延长。仅接受化疗、化疗联合不带CAR的R4‑iNKP细胞或化疗联合输注成熟的CAR‑R4iNK细胞的系列对照组均出现100%肿瘤复发。综上,CAR‑R4iNKP输注后可以体内发育为成熟的CAR‑R4iNK细胞,联合化疗可有效清除MRD,显著降低肿瘤复发率。
细胞因子诱导的记忆样NK(memory-like NK, MLNK)细胞是一类经IL-12、IL-15及IL-18短时预激活后产生的具有免疫记忆特征的NK细胞亚群,其体内持久性显著优于传统NK细胞(Rizwan Romee, et al. Blood, 2012; Rizwan Romee, et al. Science translational medicine, 2016)。该研究比较了健康人外周血制备的CAR-NK(Auto-PBMC-CD19CAR-NK)细胞、CAR-MLNK(Auto-PBMC-CD19CAR-MLNK)细胞和同一人iPSC来源的iPSC-CD19CAR-R4iNKP细胞输注治疗肿瘤的效果。结果显示,iPSC-CD19CAR-R4iNK细胞的体内持久性均显著优于Auto-PBMC-CD19CAR-NK细胞和Auto-PBMC-CD19CAR-MLNK细胞。在联合化疗清除肿瘤MRD方面,iPSC-CD19CAR-R4iNKP细胞输注组的小鼠获得了长期缓解,而接受Auto-PBMC-CD19CAR-NK细胞和Auto-PBMC-CD19CAR-MLNK细胞输注的小鼠均出现肿瘤复发。这一遗传学严谨对照结果进一步证明CAR-iNKP细胞克服了传统CAR-NK细胞的体内存续性瓶颈。
研究团队继小鼠iT细胞、iB细胞和多血液免疫谱系体内再生成功后,在人类NK细胞再生领域再次证实“体外育种,体内发育成熟”两步法再生策略的通用性。该两步法策略为未来开发更多干细胞来源的人类血液及免疫祖细胞制剂并开展临床转化测试提供了理论支持。
中国科学院动物研究所、北京干细胞与再生医学研究院王金勇研究员为论文最后通讯作者。北京干细胞与再生医学研究院胡房晓副研究员,中国科学院动物研究所张梦云副研究员及王童洁副研究员为论文共同通讯作者。共同第一作者包括:中国科学院动物研究所博士研究生王智乾、张乐强,北京干细胞与再生医学研究院副研究员黄德浩和夏成祥,高级工程师翁启童,以及中国科学院动物研究所博士毕业生林云轻。该研究在国家自然科学基金原创探索计划项目(82450001)、国家重点研发计划(2024YFA1108302)、国家卫健委四大慢病重大专项(2023ZD0501200),以及国家自然科学基金青年项目C类和面上项目(82300132、32300676、82470120)共同资助下完成。
原文链接:https://doi.org/10.1016/j.stem.2026.01.013
关键词:PSC, CXCR4, CAR-iNKP, MRD

图1
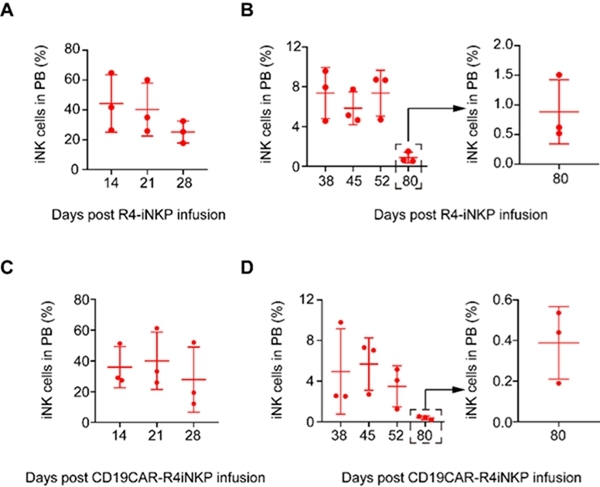
图2 iNK/CAR-iNK细胞在体内的存续时间超过80天
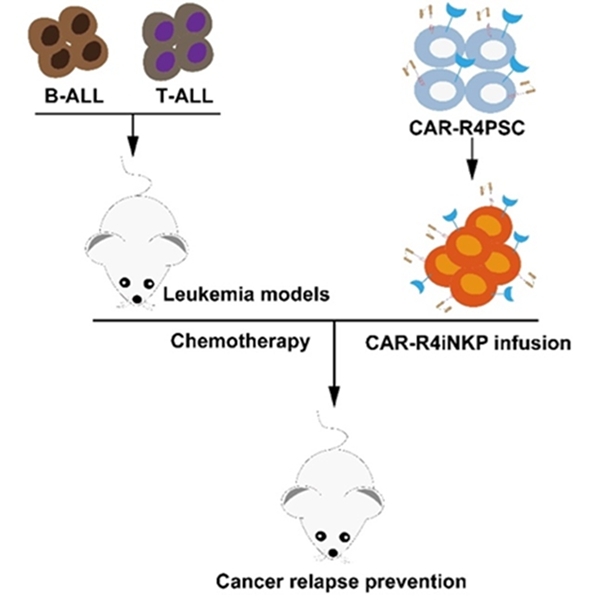
图3 CAR-iNKP细胞疗法示意图 image by WANG Jinyong lab

海南长臂猿(Nomascus hainanus)是全球最稀有灵长类,被列为国家一级重点保护野生动物,国际自然保护联盟(IUCN)物种红色名录“极危(Critically Endangered)”物种,也是海南热带雨林国家公园的旗舰物种。受...
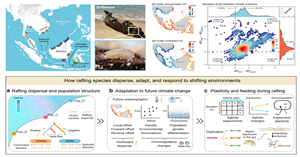
漂流扩散(Rafting dispersal)被认为是海洋物种在气候变化驱动下追踪适生生态位的重要方式。然而,物种如何在跨越漫长距离的漂流过程中,适应海洋环境波动以及应对未来气候变化,仍然缺乏深入了解。
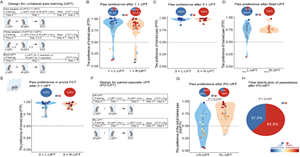
“少成则若性也,习惯成自然也。” —— 《孔子家语?七十二弟子解》 全球约90%的人是右利手(俗称“右撇子”),这一特征在不同地区与族群中高度一致。长期以来,家族内利手分布的高度相似性,使“利手由先天决定...

