生物制造研究组取得生物打印领域进展
生物打印作为组织工程与再生医学的重要技术方向,正不断推动类天然组织构建和生物制造转化研究发展。近日,顾奇团队围绕生物材料创新、干细胞生物打印策略及下一代制造技术三个关键维度,先后发表三篇相关的综述与研究论文,分别聚焦干细胞生物打印如何弥合工程组织与天然组织之间的差距、海洋来源胶原蛋白的再生医学应用潜力,以及支持贴壁细胞“即取即用”式生物3D打印的冷冻保护型生物墨水平台开发。
一、干细胞生物打印:从工程构建走向发育驱动
2026年3月12日,顾奇以独立作者身份在《Advanced Materials》发表题为《Advancing Stem Cell Bioprinting to Bridge Engineered and Natural Tissue Constructs》的综述文章,系统总结了干细胞与生物打印融合在推动功能性组织与器官构建中的新进展,并进一步提出了从“工程构建”走向“发育驱动”的新框架,为未来功能性组织制造的发展方向提供了新的理论视角。
人体器官结构高度复杂,如何精准复现其组织结构与生理功能,始终是组织工程与再生医学领域面临的核心挑战。尽管传统生物3D打印技术已能够构建一定程度的空间结构,但在模拟器官的动态发育过程及完整功能方面仍存在明显不足。干细胞因具备强大的分化潜能及对微环境信号的高度响应能力,为突破这一瓶颈提供了新的思路。文章指出,将干细胞作为“活体生物墨水”,并结合生物材料与打印策略,可在三维空间中实现其精准排布,同时构建具有支撑与调控作用的微环境。在此基础上,干细胞能够感知并整合生化与生物物理信号,发生原位分化与形态重塑。由此,打印结构不再只是静态支架,而有望重现自然发育中的部分关键过程,例如图案形成、组织极性建立和血管生成,为药物筛选、疾病模型构建以及未来器官移植带来新的可能。
文章链接:https://doi.org/10.1002/adma.202510110
二、海洋胶原开启再生医学新路径:优势显著,转化仍待突破
2026年3月18日发表在《Bioactive Materials》上的综述论文《Marine collagen for regenerative medicine: Structure–function advantages, limitations, and translational pathways》系统梳理了海洋胶原在再生医学中的应用潜力与挑战,为开发新一代生物材料提供了重要参考。文章指出,相较于传统哺乳动物来源胶原,海洋胶原在来源安全性、免疫原性低以及可持续获取方面具有显著优势。其独特的分子结构赋予材料更优的生物相容性和可调控性,在组织修复、伤口愈合及器官工程等领域展现出广阔应用前景。然而,海洋胶原也面临稳定性不足、机械性能较弱等关键限制,制约了其在复杂组织工程中的应用。研究进一步总结了通过化学修饰、复合材料设计及先进加工技术提升其性能的多种策略。在转化层面,作者强调需打通从基础研究到临床应用的关键路径,包括标准化生产、质量控制及监管审批等,以推动海洋胶原从实验室走向临床。
总体来看,该研究不仅明确了海洋胶原的结构-功能优势,也为其在再生医学中的规模化应用提供了清晰的发展方向。
文章链接:https://doi.org/10.1016/j.bioactmat.2026.03.013
三、冷冻保护型生物墨水实现贴壁细胞“即取即用”生物3D打印
2026年3月11日顾奇团队在《Advanced Materials》发表《Cryopreservative Bioink Enables Direct Bioprinting of Adherent Cells》研究论文。团队开发集成冻存与打印功能的生物墨水平台CAMP(Cryopreservation for Adhesion and Maintenance Printing),首次实现无DMSO条件下贴壁细胞的冻存与解冻后直接 生物3D打印。这项研究的核心突破在于攻克传统冻存与生物3D打印融合的两大核心问题:一是冻存过程中重结晶导致的细胞活力丧失与水凝胶结构破坏,二是冻存后细胞贴壁形态丢失、功能受损的问题。团队设计的CAMP系统采用“微载体-冻存基质”结构,将具有凹陷形貌的透明质酸微载体(cHAMCs)与改性海藻酸盐冻存基质结合,通过氢键介导的水分子固定作用抑制冰晶重结晶,其冰晶重结晶抑制能力较磷酸盐缓冲液提升约10倍,无需添加任何有毒冻存保护剂即可实现约80%的细胞存活率。此外,预培养在微载体上的贴壁细胞在冻存、复苏与打印全过程中能保持完整的黏着斑与细胞骨架伸展形态,从根本上解决了传统冻存中细胞脱壁的难题。
此外,在大鼠股骨缺损修复实验中,冻存后的CAMP构建体植入体内3个月,MicroCT结果显示骨缺损得到有效修复,验证了其优异的体内再生效果。
该技术为构建“现货型”(off-the-shelf)细胞打印体系提供新思路,有望推动标准化、规模化的组织工程制造。同时,也为临床快速响应场景(如创伤修复与个性化医疗)提供更高效的解决方案。总体来看,该研究突破了细胞储存与打印构建之间的应用瓶颈,为生物3D打印从实验室走向应用端提供重要技术支撑。
综合来看,这三项进展从“材料-细胞-制造”出发,分别聚焦再生医学中的关键环节:材料来源与性能、组织功能构建以及生产流程效率。未来,随着三者的深度融合,有望推动再生医学从实验室探索迈向临床应用,实现真正意义上的器官智造。
文章链接:https://doi.org/10.1002/adma.72714
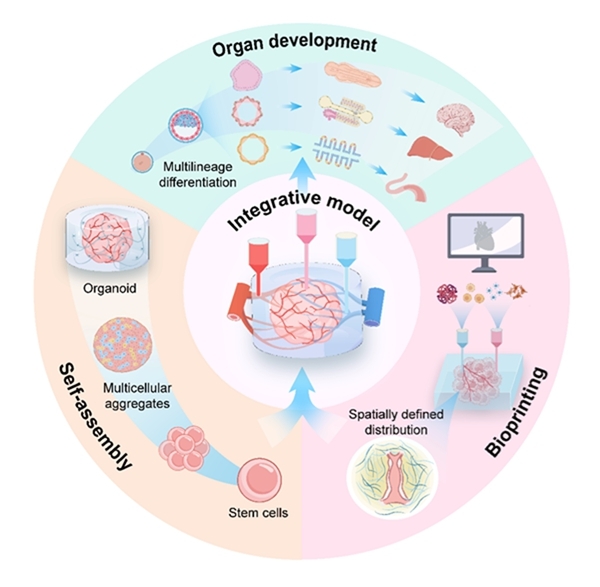
图1. 人体器官发育的生物打印技术
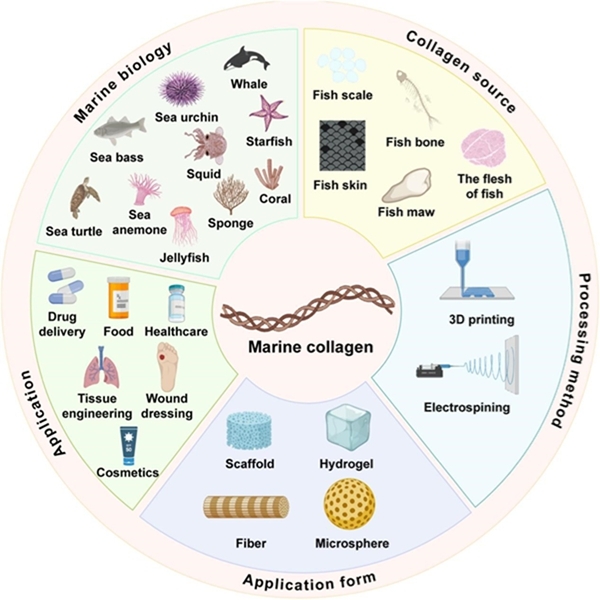
图2. 海洋胶原蛋白来源、加工策略及应用示意图
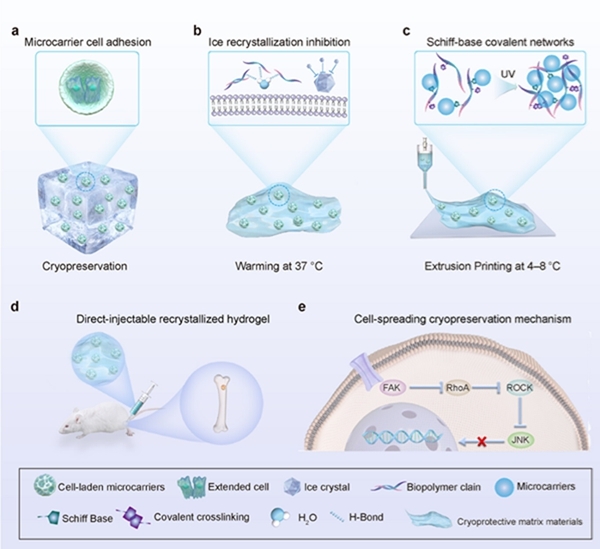
图3. CAMP系统工作流程
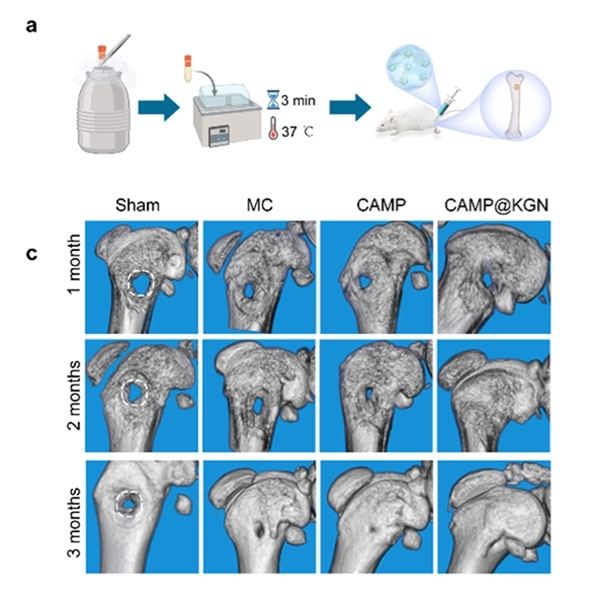
图4. CAMP应用于骨缺损治疗
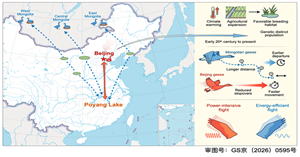
动物迁徙是自然界最壮观的现象之一。通过在广阔时空范围内追踪资源,迁徙动物能够在繁殖地与越冬地之间往返,以适应季节性环境变化。不同种群可表现出完全迁徙、部分迁徙或全年留居等不同策略,而这些策略背后反...
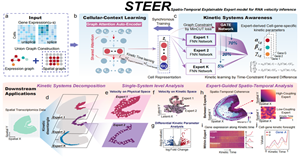
在复杂生命系统中,细胞状态会随着发育、组织重塑和疾病演化不断变化。RNA速度分析(RNA velocity)为从静态转录组数据中推断细胞状态演进趋势提供了重要手段。然而,在真实生物组织中,往往存在多种细胞动态过程...
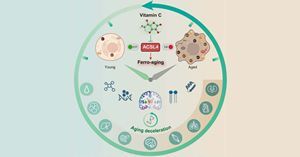
衰老是慢性疾病的首要风险因素。半个多世纪前提出的“自由基衰老理论”将氧化损伤与衰老联系起来,在衰老研究中产生了深远影响。然而,基于该理论的广谱抗氧化干预与健康获益之间的关联尚存争议,促使学界重新审...

