郑爱华研究团队探索用蚊子免疫野生蝙蝠
中国科学院动物研究所郑爱华研究组联合武汉病毒所单超团队发表题为“Ecological vaccination: A strategy to prevent zoonotic spillover from bats”的研究论文,基于One health理念,创新性地提出了一种利用自然生态行为的野生蝙蝠疫苗递送策略。该研究利用蚊子吸血、蝙蝠捕食蚊子以及蝙蝠寻盐的本能,实现重组水疱性口炎病毒(rVSV)载体疫苗的自然递送。成功在实验室及模拟野外环境中实现了对蝙蝠的有效免疫,为从源头阻断狂犬病和尼帕等人兽共患病的溢出提供了全新的解决方案。
蝙蝠既是众多人兽共患病和新发传染病的自然宿主,也是生态系统中不可或缺的关键物种,在害虫控制、作物授粉等方面发挥着重要作用。而且,很多蝙蝠本身也面临传染病的危害,比如真菌引起的白鼻综合征导致北美蝙蝠大面积死亡,严重威胁蝙蝠种群。对野生蝙蝠种群进行免疫接种,是保护蝙蝠和阻断病毒溢出风险最理想的主动防御手段。但由于蝙蝠种群庞大、飞行能力强、栖息环境复杂(如深山洞穴、高大树冠),传统的注射或诱饵投喂方式难以大规模实施。如何安全、高效地将疫苗递送给野生蝙蝠,成为全球科学界亟待解决的难题。
蚊子与蝙蝠在自然界存在密切的关系,蝙蝠体表毛发短小,血管丰富是蚊子的理想吸血宿主,蚊子也是食虫蝙蝠的重要食物。rVSV病毒载体是非常有效的疫苗载体,也是一种虫媒病毒,可以高效的感染蚊子,并且分泌到蚊子的唾液。团队构建了表达狂犬病或尼帕病毒抗原的rVSV疫苗,并通过人工喂血将其感染经X光不育处理的埃及伊蚊。对于食虫蝙蝠,通过携带疫苗的蚊子叮咬或捕食携带疫苗的蚊子实现免疫;对于果蝠,仅通过携带疫苗的蚊子叮咬也可实现免疫。实验结果显示,该策略能诱导蝙蝠产生高水平的中和抗体,有效抵御致死剂量的病毒攻击。
对于难以释放蚊子的环境,利用蝙蝠在野外普遍存在的寻盐行为,研究团队设计了一种盐雾生成装置吸引嗅觉灵敏的蝙蝠来饮用含有疫苗的盐水。在北京的矿洞模拟实验证明,该方法能有效吸引洞内的蝙蝠来饮用盐水,且操作简便、成本低廉。
该研究首次在功能上验证了利用蚊子载体和盐水陷阱对野生蝙蝠进行免疫的可行性。这不仅为狂犬、尼帕等蝙蝠源传染病的防控提供了可扩展、低成本的工具,也为保护蝙蝠种群免受白鼻综合征等疾病威胁提供了新思路。该成果是“同一健康”理念在传染病源头防控中的一次重要实践,展示了生态学与免疫学交叉融合的巨大潜力,为推进新发传染病从“溯源”推进到“防护”提供重要方案。
该工作由中国科学院动物研究所郑爱华团队和武汉病毒所单超团队牵头,联合昆明医科大学和河南师范大学等科研单位,并得到吉林和元生物工程有限公司和北京民海生物科技有限公司等疫苗公司的大力支持,第一作者为李虹悦博士、袁菲博士和姚艳丰博士。项目支持:国家自然科学基金委员会与广东省联合基金(U24A20363),国家重点研发计划(2024YFC2607505),海南热带雨林保护研究项目ZDYF2023RDYL01(依托单位:海南国家公园研究院HINP,项目编号KY-24ZK02)。
全文链接:https://www.science.org/doi/epdf/10.1126/sciadv.aec0269

图:北京郊区矿洞中一只马铁菊头蝠正在试图捕食一只落在身上的淡色库蚊。摄影:周达康
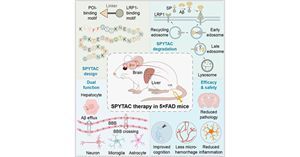
阿尔茨海默病(Alzheimer’s disease,AD)是最常见的神经退行性疾病,影响着全球约5700万人口。其典型病理特征为β-淀粉样蛋白(Aβ)在大脑中的异常沉积。这些沉积物被认为是驱动疾病发生发展的关键因素。近年...

脂质纳米颗粒(Lipid Nanoparticle,LNP)现已成为体内mRNA递送的主流技术,在传染病疫苗、蛋白替代疗法、癌症治疗及基因编辑等领域展现出了广阔的应用前景。mRNA-LNP主要通过内吞途径进入细胞,并被转运到早期内...
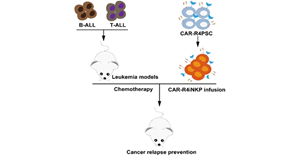
CAR-NK细胞在疾病治疗中展现出安全和通用的优势,但疗效不理想。临床上,为了提高CAR-NK细胞疗效,多采用高剂量、多剂次输注给药的策略,这导致治疗成本显著增加,加重患者经济负担。因此,传统的人体组织来源CAR...

