焦建伟团队揭示神经细胞调控血脑屏障建立的关键机制
血脑屏障是分隔血液循环与中枢神经系统的核心功能界面,其精密的结构与功能是维持大脑稳态的基石。血脑屏障的发育异常与多种重大神经系统疾病密切相关,然而,人类血脑屏障在胚胎期如何建立、其核心调控细胞与分子机制是什么,这些基本科学问题长期以来亟待解答。
2026年3月23日,中国科学院动物研究所焦建伟团队在Cell Stem Cell期刊在线发表题为Decoding the spatiotemporal development of blood-brain barrier in human cortex 的研究论文。该研究首次系统解析了人类胚胎期血脑屏障的完整发育过程,并突破性地揭示了神经前体细胞与神经元作为核心调控者,通过两条独立的信号通路分别驱动脑内皮细胞功能特化与壁细胞增殖,从而协同调控血脑屏障建立的全新机制。这一发现为理解血脑屏障发育生物学及开发相关疾病治疗策略提供了全新的理论框架。
为解析人血脑屏障的动态发育过程,研究团队整合单细胞转录组与空间转录组技术,对妊娠6至21周的人胚胎脑组织进行了系统分析。研究首次明确了人脑内皮细胞的血脑屏障关键特征在妊娠第8周开始启动,为后续机制探索确定了关键时间窗口。
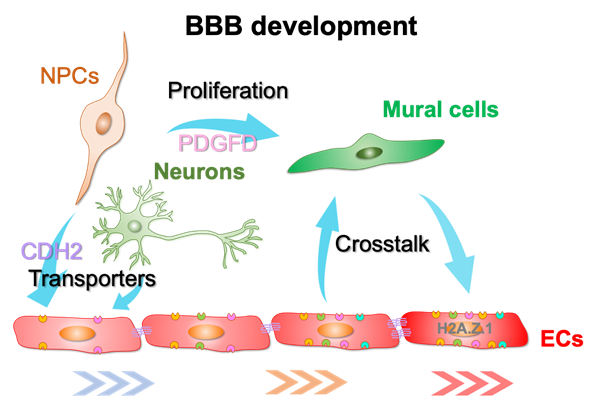
该研究的核心突破在于阐明了神经细胞不可替代的调控作用。团队发现,在发育关键期,神经前体细胞和神经元与脑内皮细胞空间毗邻,构成了其功能特化的核心微环境。通过深入机制解析,研究首次鉴定出一条不依赖于经典Wnt信号的全新通路:神经细胞通过其表面分子CDH2,与内皮细胞的CDH2直接互作,从而特异性激活内皮细胞内的β-catenin信号,驱动血脑屏障核心功能蛋白的表达。这一发现突破了领域内对血脑屏障调控机制的固有认知。
同时,研究还首次揭示了神经前体细胞对血脑屏障另一核心组分——壁细胞的调控机制。研究发现神经前体细胞通过分泌PDGFD,激活壁细胞表面的PDGFRB受体,直接促进后者的增殖,从而为血脑屏障结构的成熟与稳定提供了必要支撑。
此外,研究通过跨物种比较,揭示了人与小鼠血脑屏障发育过程的整体保守性,并鉴定出组蛋白变体H2A.Z.1在该过程中的关键作用,为利用模式动物进行后续转化研究提供了重要依据。
综上所述,该研究系统阐明了人类血脑屏障的发育过程,并创新性地提出了神经细胞通过“双通路协同”模式主导其建立的核心理论。这项工作不仅填补了领域内的重要知识空白,也为未来靶向血脑屏障治疗卒中、阿尔茨海默病等重大脑疾病,以及优化脑部药物递送策略,开辟了全新的研究方向。
中国科学院动物研究所焦建伟研究员、广州国家实验室董骥研究员、中国医学科学院基础医学研究所李妍昕研究员(原焦建伟课题组博士后)为该研究的通讯作者。郑州大学医学前沿交叉学院与第五附属医院特聘教授李忠秋(原焦建伟课题组博士后)、李妍昕研究员、董骥课题组博士研究生何梓卿为该研究的共同第一作者。研究获得了国家自然科学基金、国家重点研发计划等项目的资助。
https://doi.org/10.1016/j.stem.2026.02.010
(示意图:神经细胞调控BBB发育的关键机制)

全球性的新发传染病频繁发生,想起2019年底的新冠我们仍心有余悸,导致2026年初的几例印度尼帕的病例也会掀起轩然大波。面对这些致命的蝙蝠病毒,我们只能被动的应对吗?中国科学院动物研究所郑爱华研究组联合武...
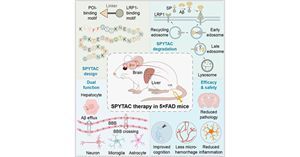
阿尔茨海默病(Alzheimer’s disease,AD)是最常见的神经退行性疾病,影响着全球约5700万人口。其典型病理特征为β-淀粉样蛋白(Aβ)在大脑中的异常沉积。这些沉积物被认为是驱动疾病发生发展的关键因素。近年...

脂质纳米颗粒(Lipid Nanoparticle,LNP)现已成为体内mRNA递送的主流技术,在传染病疫苗、蛋白替代疗法、癌症治疗及基因编辑等领域展现出了广阔的应用前景。mRNA-LNP主要通过内吞途径进入细胞,并被转运到早期内...

