中科院动物所开发出快速精准的核酸检测技术
高效精准的核酸检测技术在传染病原检测、食品安全检疫和致病基因筛查等许多方面具有重要的应用。基于CRISPR的基因组编辑技术极大地革新了生物医学研究。有趣的是,除了能够通过对基因组精准操控来进行功能基因组学研究,最近一些研究发现CRISPR系统的某些效应蛋白,例如Cas12a,在切割靶DNA后会受激获得切割非靶向单链DNA(ssDNA)的活性,从而能够用于快速简便地进行核酸检测,在传统的PCR和测序技术之外建立了一种新的核酸检测技术。
CRISPR-Cas12b/C2c1系统大多来自嗜热菌,由于其嗜高温的特性研究相对较少。中国科学院动物研究所李伟研究团队在2018年首次成功地改造Cas12b系统用于哺乳动物基因组编辑,建立了Cas9和Cas12a之后的第三个CRISPR基因编辑工具[1]。在此基础上,研究团队发现Cas12b蛋白在激活之后同样具有任意切割ssDNA的特性,并开发出 CDetection(Cas12b-mediated DNA detection)检测系统,可以用于微量DNA的简便快速的检测。CDetection是集Cas12b蛋白、向导RNA、ssDNA荧光报告分子和 RPA(recombinase polymerase amplification)等温扩增于一体的DNA快速检测系统。Cas12b蛋白在靶向切割RPA扩增目标DNA后激活ssDNA切割活性,任意切割ssDNA荧光报告分子,从而发出荧光信号(图1)。基于团队前期研究发现的Cas12b能够适应较广温度(25~60℃)和pH(1~8)的稳定性,CDetection系统相较Cas12a-DETECTR系统具有更高的灵敏度,可以实现亚aM(10-19 M)的灵敏DNA检测;同时,通过tgRNA(tuned gRNA)的引入,CDetection可以实现单碱基的区分。利用CDetection系统,能够快速地实现细胞、血液、尿液以及动植物中的细菌和病毒感染、基因分型以及SNP突变检测(图1)。
相关成果于2019年7月2日在国际学术期刊Genome Biology发表 [2]。该研究工作由中国科学院动物研究所和中国科学院干细胞与再生医学创新研究院完成。中国科学院动物研究所李伟研究员和周琪研究员为论文的通讯作者;博士生滕飞、郭璐为共同第一作者。该研究受到中科院战略科技先导专项及科技部、基金委等项目的资助。
[1] Repurposing CRISPR-Cas12b for mammalian genome engineering
图1 CDetection实现DNA的快速精准检测
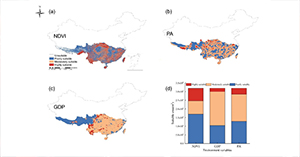
人类活动和气候变化加速生物多样性的减少,导致物种范围的转移、收缩和扩张。在全球范围内,人类活动和气候变化已对生物多样性构成了严重威胁,目前已导致全球522种灵长类动物中约68%的物种面临灭绝风险。

植物病毒素有“植物顽疾”之称,每年引起全球作物经济损失高达4000亿元。水稻作为人类重要的粮食作物之一,供给全世界一半以上的人口,主要种植于亚洲、非洲和南美洲等地区。

