新冠病毒鼻喷疫苗研究取得新进展
近日,中国科学院动物研究所郑爱华研究组联合军事医学科学院微生物流行病研究所秦成峰研究组并与中国科学院动物研究所实验动物中心多曙光博士合作,在基于水疱性口炎病毒载体的新冠病毒鼻喷疫苗研究开发方面取得进展。相关研究成果近期在Signal Transduction and Targeted Therapy杂志发表。
随着多款灭活疫苗、mRNA疫苗、亚单位疫苗和腺病毒载体疫苗获批,各国在努力提高疫苗接种率。但随着突变株的不断产生,新冠疫苗暴露出免疫原性差和保护率降低等问题,突破感染越来越严重,如何提高疫苗的保护效果是目前面临的巨大挑战。水疱性口炎病毒VSV(Vesicular stomatitis virus)是弹状病毒科的模式毒种。作为一种新兴的活载体疫苗,VSV具有易于培养、安全高效、易使用、不受人体预存免疫的影响、能刺激机体产生强烈的细胞和体液免疫反应等特点。2019年欧盟和美国分别批准默沙东公司基于VSV载体开发的埃博拉疫苗上市,效果显著。VSV成为最有希望的活病毒载体之一。
通过将VSV的G蛋白置换成新冠病毒的S蛋白,郑爱华研究组构建了可复制的rVSV-SARS-CoV-2载体疫苗,并于2020年3月申请了专利。本研究中,研究人员评估了在非人灵长类中不同的免疫方式对rVSV-SARS-CoV-2免疫原性的影响。结果表明,喷鼻免疫所诱导的中和抗体水平比肌肉注射高8倍。因此,rVSV-SARS-CoV-2更适合开发成喷鼻疫苗。
SARS冠状病毒与新冠病毒具有亲缘关系,二者刺突蛋白(Spike, S)氨基酸序列75%相同,而且细胞受体都是ACE2。然而,SARS病人相对新冠病人体内产生的中和抗体滴度更高,且持续时间更长。为了提高疫苗的免疫原性,本研究先构建了表达SARS冠状病毒S蛋白的复制型rVSV-SARS-CoV,在此基础上,把SARS冠状病毒的RBD置换成新冠病毒的RBD,获得了表达新冠主要免疫原的嵌合疫苗株rVSV-SARS-CoV/2-RBD(图1)。在小鼠、仓鼠和食蟹猴模型里,嵌合株rVSV-SARS-CoV/2-RBD的抗新冠病毒中和抗体水平约为rVSV-SARS-CoV-2的3倍。单次免疫两种疫苗均可以有效的保护hACE2小鼠模型免受新冠病毒的感染,且嵌合疫苗株rVSV-SARS-CoV/2-RBD的效果明显优于rVSV-SARS-CoV-2(图2)。
这些结果为rVSV-SARS-CoV/2-RBD作为SARS-CoV-2的有效候选疫苗的开发奠定了基础。在SARS冠状病毒S中嵌合表达SARS-CoV-2 S RBD的策略也为其他疫苗平台的设计提供了新思路。
中国科学院动物研究所研究生李虹悦、张毓航,深圳康泰生物技术有限公司李东,军事医学科学院微生物流行病研究所邓永强副研究员和郑州大学徐洪德副教授为本文共同第一作者。中国食品药品检定研究院黄维金研究员和中国科学院生物物理研究所郝俊峰副研究员提供了重要技术支持。
论文链接:https://www.nature.com/articles/s41392-021-00797-9。

图1:rVSV-SARS-CoV/2-RBD疫苗设计示意图

图2:rVSV-SARS-CoV-2与rVSV-SARS-CoV/2-RBD对hACE2小鼠的保护效果
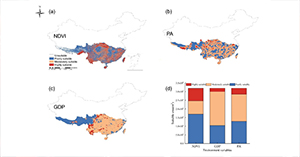
人类活动和气候变化加速生物多样性的减少,导致物种范围的转移、收缩和扩张。在全球范围内,人类活动和气候变化已对生物多样性构成了严重威胁,目前已导致全球522种灵长类动物中约68%的物种面临灭绝风险。

植物病毒素有“植物顽疾”之称,每年引起全球作物经济损失高达4000亿元。水稻作为人类重要的粮食作物之一,供给全世界一半以上的人口,主要种植于亚洲、非洲和南美洲等地区。

