王德华和张学英团队揭示了荒漠啮齿动物通过“菌群-肠-肾”轴耐受高盐的机制
人类长期高盐饮食易引起高血压、心脏病、肾脏病和脑出血等一系列疾病,但有些动物物种在野外环境中终生取食高盐植物,却能够保持健康。例如,生活在荒漠地区的啮齿动物长爪沙鼠(Meriones unguiculatus),不仅耐高温,也能耐受高盐食物,所取食的植物盐含量可超过10%(海水的盐度一般为35‰),这些沙鼠具有极强的节水和耐盐能力。肾脏能够清除代谢废物并重吸收水分,是重要的水/盐代谢器官。我们在前期工作中发现,长爪沙鼠具有较高的肾脏髓质厚度和水分重吸收能力,可产生高度浓缩的尿液,在禁水或者高盐饮水条件下尿液渗透压可达7000 mOsm/kg以上(正常饮食饮水的沙鼠,尿液渗透压为600-2000 mOsm/kg,Xu and Wang, 2016; Nouri et al., 2020)。那么荒漠啮齿动物节水和耐盐的生理机制是怎样的呢?
2022年4月4日,中国科学院动物研究所王德华和张学英研究团队在国际期刊npj Biofilms and Microbiomes上发表题为“The microbiota-gut-kidney axis mediates host osmoregulation in a small desert mammal”的研究论文,发现了肠道菌群与宿主肾脏对高盐诱导的水盐代谢的调节作用,阐明了“菌群—肠—肾”轴对荒漠啮齿动物耐受高盐的调节机制。
在这项工作中,研究人员通过对长爪沙鼠饲喂正常鼠饲料,分别进行4%或8%的高盐饮水处理4周诱导高盐缺水模型,以研究高盐缺水引起的肾脏和肠道生理和肠道微生态的变化;另外对8%高盐摄入的动物移植正常动物来源的肠道菌群,并继续饮用8%的高盐水,以研究正常动物的肠道菌群是否能够缓解高盐摄入引起的损伤。研究发现,高盐摄入导致动物的摄食量和饮水量明显降低,动物处于负能量平衡状态,并产生少量的高度浓缩尿;高盐动物通过提高肠道和肾脏组织上皮细胞中水通道蛋白2(AQP2)的表达增加细胞对水分的重吸收,降低α-钠通道蛋白(α-ENaC)的表达提高细胞的排钠能力。高盐摄入引起肠道菌群的多样性降低,菌群组成结构发生改变,特定细菌如理研菌属(Rikenella)和克里斯坦森氏菌(Christensenella,具有降低胆固醇功能)的相对丰度明显降低,而与炎症和结直肠癌有关的阿托波氏菌属(Atopobium)明显升高,血清炎症因子水平明显升高(图1)。菌群移植能够重塑肠道微生态,例如罗伊氏乳杆菌(Lactobacillus reuteri)明显升高,而狄氏副拟杆菌(Parabacteroides distasonis)和普雷沃氏菌属(Prevotella copri)相对丰度明显降低,这些特定细菌的变化伴随丁酸盐浓度明显升高,而乙酸盐浓度相对降低;移植正常菌群的高盐动物能量代谢、渗透调节和炎症水平等得以恢复或缓解(图2)。该研究阐明了“菌群—肠—肾”轴对荒漠啮齿动物耐受高盐的调节机制,揭示了肠道菌群与宿主的协同进化对动物能量代谢、水盐调节的重要生理意义,为人类高盐饮食对机体危害的预防和治疗提供理论依据和可能的干预措施。
中国科学院动物研究所博士研究生Zahra Nouri和张学英副研究员为论文共同第一作者,中国科学院动物研究所、中国科学院生物互作卓越创新中心研究员、山东大学生命科学学院教授王德华和中国科学院动物研究所副研究员张学英为论文共同通讯作者。博士生Saeid Khakisahneh和以色列本·古里安大学的Allan Degen教授参与了本项研究。该研究得到了国家自然科学基金委项目和中国科学院B类先导科技专项培育项目的资助。
文章信息和链接:Nouri Z, Zhang XY, Khakisahneh S, Degen AA, Wang DH. 2022. The microbiota-gut-kidney axis mediates host osmoregulation in a small desert mammal. npj Biofilms and Microbiomes. 8:16.
https://doi.org/10.1038/s41522-022-00280-5or as a PDF here https://www.nature.com/articles/s41522-022-00280-5.pdf.

图1 菌群移植重塑肠道微生态缓解高盐诱导的渗透调节压力

图2 “菌群—肠—肾”轴介导高盐诱导的渗透调节的模式图
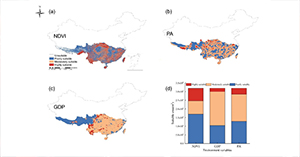
人类活动和气候变化加速生物多样性的减少,导致物种范围的转移、收缩和扩张。在全球范围内,人类活动和气候变化已对生物多样性构成了严重威胁,目前已导致全球522种灵长类动物中约68%的物种面临灭绝风险。

植物病毒素有“植物顽疾”之称,每年引起全球作物经济损失高达4000亿元。水稻作为人类重要的粮食作物之一,供给全世界一半以上的人口,主要种植于亚洲、非洲和南美洲等地区。

